Stai per scoprire la reazione di Ozonolisi di un alchene con ben 3 esercizi svolti e commentati. Te la mostrerò con diverse molecole di partenza, in modo tale che vedrai le diverse possibilità che ti potrebbero capitare al compito.
Premessa sull’Ozonolisi: risonanza dell’ozono, ed i reagenti
Spesso i professori chiedono innanzitutto di disegnare le strutture di risonanza dell’ozono (O3). Le ho già mostrate in una guida in cui parlavo di strutture di risonanza. Ma te le mostro nuovamente. Ti do anche qualche consiglio per ricordarle.
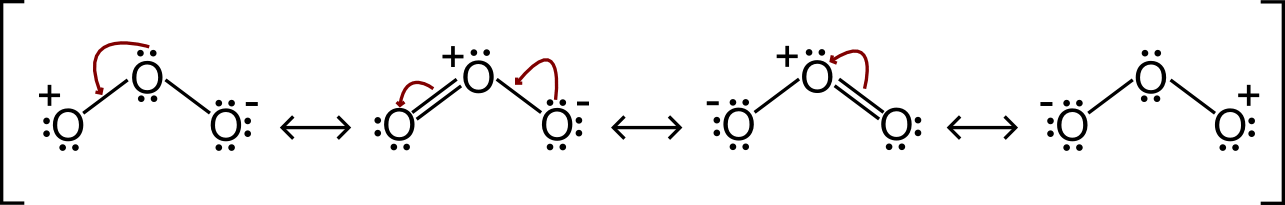
Guarda bene innanzitutto che la prima e la quarta struttura di risonanza sono speculari. Poi ti consiglio di scrivere bene gli elettroni nella prima struttura (le altre verranno di conseguenza).
Adesso, devi ricordare che c’è una carica positiva nell’ossigeno di sinistra, così gli elettroni si muovono (facendo un doppio legame) per neutralizzarla. Anche nelle altre strutture sarà tutto un “gioco” in cui gli elettroni si muoveranno per neutralizzare la carica positiva.
Meccanismo di Reazione dell’Ozonolisi
A livello pratico, si discioglie l’alchene in un solvente inerte (es: il diclorometano) e ci si fa passare l’ozono, in condizioni di bassa temperatura (-68°C, qualche prof dice -78°C).
La molecola più semplice per mostrarti l’ozonolisi è il 2-metil-2-butene.
Quello che ti consiglio è di prendere la prima struttura di risonanza dell’oznono e di sistemarla in basso all’alchene, in modo tale che l‘ossigeno carico negativamente si trovi sotto il carbonio più sostituito (se sono sostituiti in modo uguale, è indifferente).
Nel primo stadio, l’alchene reagisce con l’ozono per formare il molozonide (o molozonuro), che è un intermedio instabile.

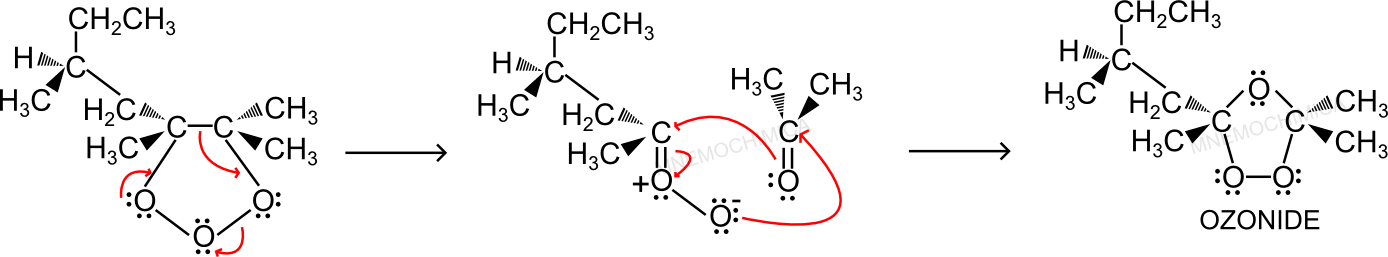
Per l’appunto, essendo il molozonide instabile, si riarrangia per formare l’ozonide che invece è più stabile.
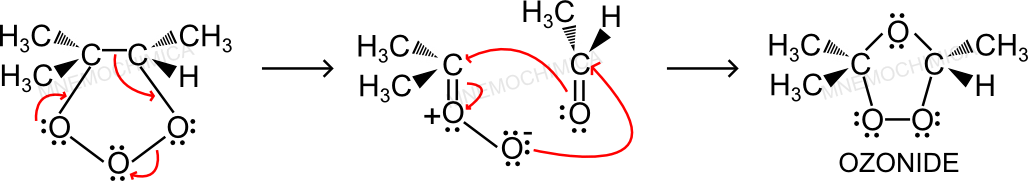
Come puoi vedere, gli elettroni di legame tra i due carboni, formano il doppio legame tra il carbonio e l’ossigeno, che a sua volta cede gli elettroni di legame all’altro ossigeno ed infine l’ultimo Ossigeno fa un’altro doppio legame. I composti formati, si addizionano per dare vita all’Ozonide (oppure Ozonuro).
A questo punto ho tre possibilità (due delle quali mi daranno lo stesso risultato):
- Zinco ambiente acido (H3O+) oppure dimetil solfuro (CH3)2S
- Acqua Ossigenata (H2O2)
L’unica differenza è che – utilizzando l’acqua ossigenata – se tra i prodotti ci sono aldeidi , al loro posto otterrò acidi carbossilici (-OH al posto di H).

Nel primo caso ottengo il 2-propanone (acetone) e l’etanale (acetaldeide). Mentre nel secondo caso, cambia solo che al posto dell’etanale, ottengo l’acido etanoico.
Non è tutto, perché voglio svelarti un segreto.
Trucco per capire i prodotti
 Il trucco mnemonico che ho ideato per vedere immediatamente i prodotti finali è questo: immagina di tagliare l’alchene nel doppio legame. Ora, al posto di fare il doppio legame con l’altro carbonio, lo fanno con l’ossigeno. Ecco, questi sono i prodotti con lo zinco in ambiente acido o con il dimetil solfuro. Mentre per l’acqua ossigenata, in più devi considerare che l’idrogeno dell’aldeide si trasforma in un OH.
Il trucco mnemonico che ho ideato per vedere immediatamente i prodotti finali è questo: immagina di tagliare l’alchene nel doppio legame. Ora, al posto di fare il doppio legame con l’altro carbonio, lo fanno con l’ossigeno. Ecco, questi sono i prodotti con lo zinco in ambiente acido o con il dimetil solfuro. Mentre per l’acqua ossigenata, in più devi considerare che l’idrogeno dell’aldeide si trasforma in un OH.
Te lo mostro in pratica.
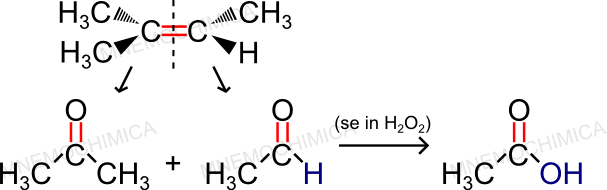
Il prodotto che si forma a sinistra (chetone), lo otterremo sia con lo Zinco che con l’acqua ossigenata. Mentre, il prodotto di destra (aldeide), solo con lo Zinco. Questo perché l’acqua ossigenata è un forte ossidante (tende a far aumentare il numero di legami con l’ossigeno), e di fatti l’H dell’aldeide si ossida a OH. Diventa quindi un Acido Carbossilico.
Altri due esercizi
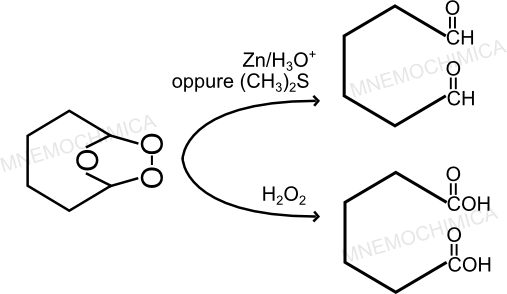
Spesso mi chiedono: “ma cosa succede se l’alchene è ciclico?” La stessa identica cosa, solo che al posto di ottenere due prodotti separati, la molecola resta unita.
Te lo mostro in pratica con un esercizio svolto e commentato sull’ozonolisi del cicloesene.

Come sempre, la molozonide è instabile, e proprio per questo motivo, si riarrangia.

Infine, come sempre, ho tre possibilità per far reagire l’ozonide.
Per l’ultimo esercizio svolto, voglio mostrarti – insieme – 2 cose che sbagliano in molti.
Immagina di avere questa bella molecola che ti ho disegnato in basso. La prima cosa che ti consiglio di fare è di assegnare il nome IUPAC al composto (con tanto di stereochimica).
Per approfondire: due guide sulla nomenclatura degli alcheni e sui centri chirali.

Ti guido io verso la soluzione. Ricorda che i carboni del doppio legame devono avere il numero più basso. Quindi inizio a contare da uno dei due carboni in basso a destra.La catena principale è lunga 7 carboni e non ne fanno parte tre gruppi metilici (sostituenti), in posizione 2,3 e 5. Inoltre, vedo che c’è anche un centro chirale, che è (S). Quindi, il nome IUPAC della molecola è (S) 2,3,5-trimetil-2-eptene.
Dove voglio arrivare a parare con questo molecolone?
lo vedrai tra poco.

A questo punto si prosegue come sempre.
A questo punto, se ci fai caso (e se ricordi il trucchetto di cui ti ho parlato prima), otterrai solo chetoni come prodotti finali, indipendentemente dal reagente che usi (si, perché non puoi ottenere aldeidi). Questo è importante da sapere, molti sono convinti che devono ottenere per forza un aldeide ed un chetone, ma non è così! Non è tutto.

Guarda bene i prodotti che hai ottenuto. Uno di loro ha un centro chirale. Era (S) ed è rimasto tale. Si, perché la reazione non ha coinvolto direttamente quel carbonio. Quindi l’unico modo in cui poteva cambiare, era un cambio nelle priorità dei sostituenti. Solo in quel caso può cambiare il centro chirale…





