In questa guida vedrai la condensazione di Claisen tra due esteri in modo estremamente pratico (cercherò anche di darti qualche nozione extra).
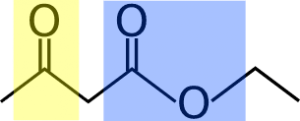
In cosa consiste questa reazione? Ci fa ottenere un β-chetoestere (che è una molecola simile a quella che vedi in basso), a partire da un estere ed un alcossido (ione di un alcol). Prima di andare avanti voglio mostrarti bene cosa significa β-chetoestere, come dice il nome, c’è una “porzione” simile ad un estere (azzurro) e nel carbonio β, c’è un gruppo chetonico (in giallo). Questa molecola in particolare si chiama estere acetacetico.
Si comincia…
Meccanismo della Condensazione di Claisen
Il primo passo è scrivere un estere di partenza, in questo esempio ti mostrerò la condensazione di Claisen, utilizzando l’etanoato di etile (nome comune: acetato di etile), in modo tale da ottenere come prodotto finale, l’estere acetacetico che ti ho mostrato prima.
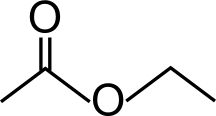
Nel primo stadio si deprotona l’estere
Il primo step è quello di deprotonare (togliere un idrogeno) l’estere, in modo tale da renderlo un nucleofilo (ed “attivarlo”) per la reazione successiva. Però fai attenzione. Ricorda che quando vai a deprotonare un estere, il carbonio da cui “prenderai” l’idrogeno, è quello in alfa. Quindi gli idrogeni disponibili sono quelli che vedi in rosso nell’immagine. Ma c’è un’altra informazione altrettanto importante…
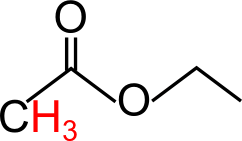
Con cosa si deprotona l’estere nella Reazione di Claisen?
![]() In genere, nelle reazioni acido-base si deprotona con una base forte come l’idrossido di sodio (NaOH), ma non in questo caso! Fai molta attenzione. Perché altrimenti avviene una reazione che si chiama saponificazione. Quindi, scarta le basi forti come l’NaOH.
In genere, nelle reazioni acido-base si deprotona con una base forte come l’idrossido di sodio (NaOH), ma non in questo caso! Fai molta attenzione. Perché altrimenti avviene una reazione che si chiama saponificazione. Quindi, scarta le basi forti come l’NaOH.
![]() Devi sfruttare un alcossido (ione dell’alcol). Ma non uno random, perché se lo fai reagire con un alcossido a caso avviene la transesterificazione (Ovvero, diventa semplicemente un altro estere).
Devi sfruttare un alcossido (ione dell’alcol). Ma non uno random, perché se lo fai reagire con un alcossido a caso avviene la transesterificazione (Ovvero, diventa semplicemente un altro estere).
![]() In definitiva, basta farlo reagire con l’alcossido corrispondente, come ti evidenzio in rosso. Ovvero quella porzione che va dall’ossigeno in poi.
In definitiva, basta farlo reagire con l’alcossido corrispondente, come ti evidenzio in rosso. Ovvero quella porzione che va dall’ossigeno in poi.
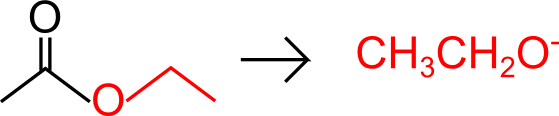
In questo caso si tratterà di un etossido (posso usare ad esempio l’etossido di sodio), che altro non è che lo ione di un etanolo.
[learn_more caption=”Approfondimento >>”] Nota bene. Qualche professore vuole vedere l’alcossido sotto forma di sale, quindi ti basterà aggiungere un Na+(sodio) vicino. Il sale in questione è appunto l’etossido di sodio (chiamto anche etilato sodico CH3CH2O- Na+ oppure direttamente CH3CH2ONa visto che la somma delle cariche è uguale a zero).[/learn_more]
Detto ciò, passo alla pratica. Quindi, come già detto, per prima cosa deprotono l’estere con l’alcossido. La reazione come vedi è sfavorita.

Il prodotto ottenuto, reagisce con un altro estere. Si ottiene così un intermedio a quattro centri.
Come puoi notare c’è una carica meno e un atomo non “si sente a suo agio” quando è carico, ma “preferisce” tornare neutro. Come fa in questo caso a neutralizzare la carica? Forma il doppio legame [ricreando di fatto carbonile (C=O)]. Il carbonio ovviamente non può fare 5 legami e deve per forza di cose rompere il legame con l’alcossido, che esce portando via gli elettroni (l’ossigeno assumerà di conseguenza la carica negativa).
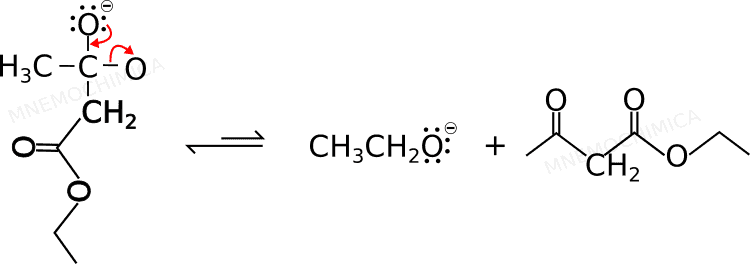
Come vedi, abbiamo già creato il prodotto finale (β-chetoestere). Tutto finito quindi? Purtroppo no.
Il problema è quel maledetto alcossido che è appena uscito. E’ una base abbastanza forte e andrà a deprotonare il β-chetoestere. Il pka dell’estere acetacetico è circa 11, mentre quello dell’alcol che si andrà a formare è di circa 16. Vediamo se hai capito, dove è spostato l’equilibrio? Verso destra.

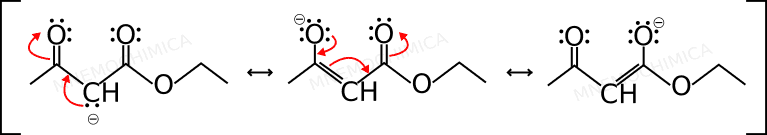
Quindi otteniamo, un alcol e lo ione di un β-chetoestere (attenzione perché ha ben tre strutture di risonanza, questo lo stabilizza come spiego nella guida sul come disporre i composti in ordine di acidità).
L’ultimo passaggio della condensazione di Claisen è abbastanza logico. Devo protonare il β-chetoestere per neutralizzare la carica negativa. Posso farlo grazie ad un acido forte (come ad esempio l’acido cloridrico, HCl) e la reazione è finita.

In sintesi, la condensazione di claisen è così: deprotono, la molecola deprotonata reagisce con l’estere di partenza, si ripristina il carbonio carbossilico mentre l’alcossido se ne va come gruppo uscente. L’alcossido appena uscito mi deprotona il β-chetoestere che provvederò a riprotonare con un acido forte.
Ti assicuro che è più semplice a farsi piuttosto che a scriverlo.
Quindi, di seguito troverai due esercizi (di cui presto inserirò), la soluzione ed i commenti. Mi raccomando, prima cerca di fare da solo l’esercizio.
Esercizi
Attenzione perché il secondo esercizio è leggermente più difficile, perché devi tenere conto della stereochimica. L’ho inserito di proposito, perché in questo modo, se ti dovesse capitare un problema simile all’esame, sai come risolverlo (ti dico come nelle soluzioni).
Descrivere la condensazione di Claisen tra due molecole di:
- etanoato di metile;
- propanoato di etile;