Grazie all’Esterificazione di Fischer, è possibile trasformare un acido carbossilico (-COOH) in un estere (-COOR). Più precisamente, si fa reagire un acido carbossilico ed un alcol in ambiente acido.
Quale estere puoi sintetizzare? Praticamente tutti, ti basterà scegliere in modo accurato i composti di partenza.
Vediamo come.
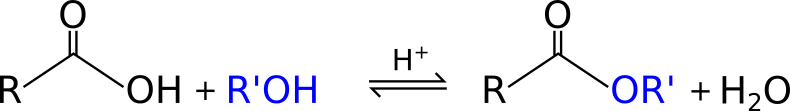
Come puoi vedere nell’estere a destra, la porzione in blu deriva dall’alcol, mentre il resto dall’acido carbossilico.
Ti faccio un esempio con composti “reali”. Parto dall’acido benzoico e voglio ottenere un benzoato di etile (estere). Come puoi vedere dalla porzione in blu, devo usare un alcol etilico (etanolo).
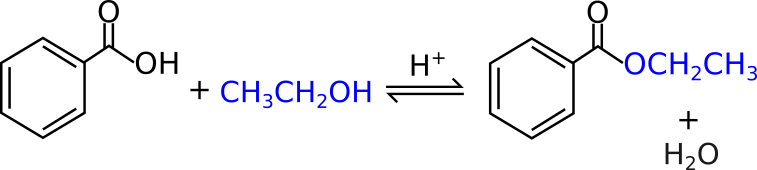
Esterificazione di Fisher: Meccanismo
Si mette l’acido carbossilico (in questo caso userò l’acido benzoico) in ambiente acido (HCl oppure H2SO4). L’acido agisce come catalizzatore, ovvero velocizza la reazione senza consumarsi.
Come agisce? Protona l’ossigeno del carbonile (C=O), perché è il più basico ed in questo modo aumenta l’elettrofilia del carbonio del gruppo carbossilico.

Il prodotto può essere scritto sotto forma di 2 strutture di risonanza. Come puoi vedere, nella seconda la carica + si trova sul carbonio. Questo spiega il perché della maggiore elettrofilia di quest’ultimo.
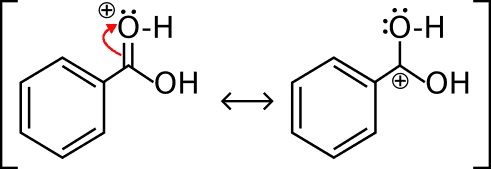
Ma veniamo al dunque, al passaggio cruciale, ovvero alla reazione con l’alcol (debole nucleofilo) che si lega al carbonio del gruppo carbossilico. Quest’ultimo non può fare 5 legami. Così gli elettroni del doppio legame vanno a finire sull’ossigeno (che così torna ad essere neutro).
Ah, per semplicità scrivo il benzene (che come sostituente si chiama fenil) come “Ph”.
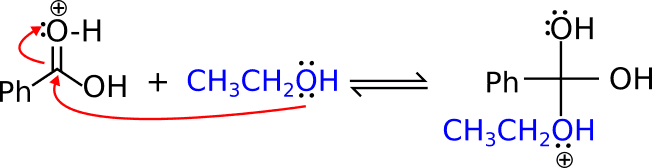
Per prima cosa pensa al fatto che l’ossigeno ha una carica positiva, che puoi neutralizzare semplicemente deprotonandolo.
Dopodiché tieni presente che devi cercare di ottenere un estere, di conseguenza ci sono troppi gruppi OH. Il modo migliore per farne uscire uno è sicuramente quello di protonarlo (legarci un idrogeno), trasformandolo così in -OH2 che è un ottimo gruppo uscente (la molecola di acqua è stabile).
In pratica è moto più semplice a rappresentarlo piuttosto che a spiegartelo.
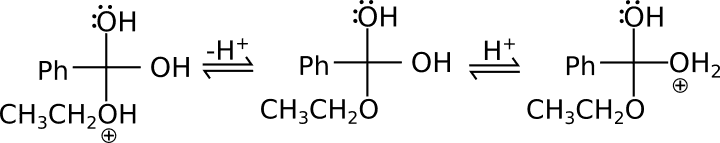
È quasi finita. Non disperare!
Ora, si concretizza il tutto.
L’ossigeno forma il doppio legame, ricreando il carbonile. Il carbonio a sua volta non può fare 5 legami e si “libera” del legame con -OH2 che esce sotto forma di acqua.
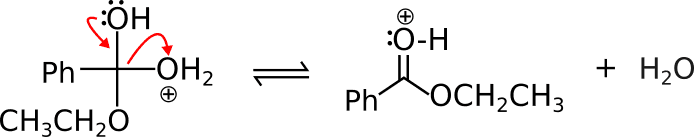
L’ultimo procedimento dell’esterificazione di Fischer è scontato, c’è una carica +, come la neutralizzi? Si, ci siamo capiti: deprotonando. Et voilà, l’estere è pronto!
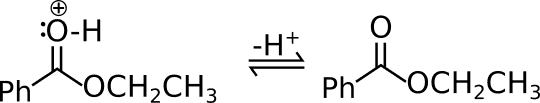
Fai tanti esercizi e ti entrerà sicuramente in mente.
Video
Ah, quasi dimenticavo, ti consiglio di guardare anche il video sull’esterificazione di Fischer. Dura poco più di 5 minuti, perché l’ho reso breve ma intenso!
Qual è il canale Youtube? Isciviti gratis qui (e poi clicca sulla campanella altrimenti YT non ti avvisa quando escono nuovi video!)
Lo trovi nella playlist “reazioni” …