Il gruppo OH (gruppo alcolico, ossidrile o meglio gruppo idrossilico, insomma, chiamalo come ti pare) lo puoi trovare negli idrossidi e negli alcoli. Così, ho deciso di scriverci una guida facile facile e soprattutto completa…
Nomenclatura
Quando il gruppo ossidrile è il principale, si tratta per l’appunto di un alcol ed il suffisso è “-olo” (esempio: metanolo, formula CH3OH). Mentre quando il gruppo OH si considera un sostituente, la dicitura è “idrossi” (esempio: acido (s) 2-idrossipropanoico).
Per approfondire: qui trovi una marea di esercizi sulla nomenclatura degli alcoli, compresi i fenoli…
Mentre per quanto riguarda gli idrossidi, questi sono dei sali che rilasciano il gruppo OH– creando di conseguenza un ambiente basico. Il nome si forma dalla parola idrossido + “di” + il metallo. Ecco qualche esempio:
- NaOH (Idrossido di sodio)
- KOH (idrossido di Potassio)
- Mg(OH)2 (Idrossido di Magnesio)
Acidità (e pka) degli alcoli
Per favore, NON dirmi che gli alcol in generale sono acidi. Lo sento spesso. Ok, posso anche capirlo per il fenolo (alcol aromatico), e/o quando vicino ci sono legati gruppi elettron attrattori (come gli alogeni), ma non per quelli “classici”.
Sai perché il fenolo è più acido? Te ne parlo stra poco.
Però prima ti mostro l’acidità del gruppo idrossilico. Sai da cosa dipende? Devi vedere come è sostituito il carbonio a cui è legato. Ovviamente ti do dei valori di pka abbastanza generici, tu affidati sempre a quelli dettati dal tuo professore (anche perché a volte i prof hanno dei valori soggettivi).
In generale si va dai un pka di circa 15,5 (per il metanolo) e si alza mano a mano che aumentano i gruppi alchilici legati al carbonio che lega il gruppo OH, fino a circa 18 (se il gruppo idrossilico lega un carbonio terziario). Ah, ovviamente considera che il pka dell’acqua è 15,7.

Fai caso ad una cosa. Più ci sono gruppi alchilici (es: -CH2CH3) che legano il carbonio e più è bassa l’acidità (alto il pka). Sai perché? Per effetto elettron donatore che hanno proprio questi gruppi. Magari te ne parlerò in un’altra pagina che scriverò a breve.
Però ricorda solo che riducono l’acidità, come è evidente anche nell’immagine sopra.
Al contrario, cosa rende il fenolo più acido?
Come già detto, il fenolo è leggermente “diverso”, infatti ha un pka di circa 10 (9,8 in realtà). Quindi – visto che si parla di una scala logaritmica – è milioni di volte più acido degli altri. Questo si spiega grazie alla stabilità dello ione coniugato.
Infatti, devi sempre considerare che più lo ione coniugato è stabile, e maggiore è l’acidità del composto.
Sai perché in questo caso la base coniugata è stabile? Grazie alle strutture di risonanza, ne ha addirittura 4. Te lo mostro sotto, dove lo deprotono genericamente indicandolo con (-H+).
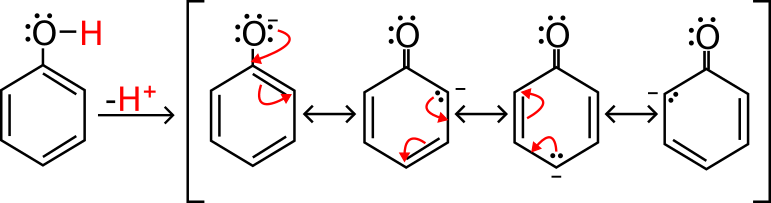
Come Gruppo Uscente
Il gruppo OH è un pessimo gruppo uscente, così come tale. Perché? Per ottimo, dovrebbe avere una bassa reattività, cosa che invece l’idrossile non ha (anzi, è proprio il contrario visto che è molto reattivo).
Proprio per questo motivo, generalmente il gruppo ossidrilico, si protona prima, in modo tale da “uscire” sotto forma di H2O, che invece è un ottimo gruppo uscente (proprio perché ha una bassa reattività).






