La sostituzione elettrofila aromatica (SEA) è una delle reazioni più importanti della chimica organica. O quantomeno lo è per me. Tieni in considerazione che è molto semplice e sopratutto che ti permetterà di ottenere una vasta gamma di possibili composti aromatici…
Indice:
- Schema
- Meccanismo di Reazione della Sostituzione Elettrofila Aromatica
- Se il benzene ha già un sostituente?
Il gruppo di reazioni che sfruttano il meccanismo della SEA, è variegato:
- Alogenazione (Clorurazione, Bromurazione, ecc);
- Alchilazione di Friedel-Craft;
- Acilazione di Friedel-Craft;
- Nitrazione;
- Solfonazione;
Ho creato uno schema che ti permetterà di vedere istantaneamente i prodotti delle varie reazioni di Sostituzione Elettrofila Aromatica. Uso come composto di partenza il benzene, perché è il composto aromatico per eccellenza (oltre ad essere la molecola più usata nei vari compiti d’esame).
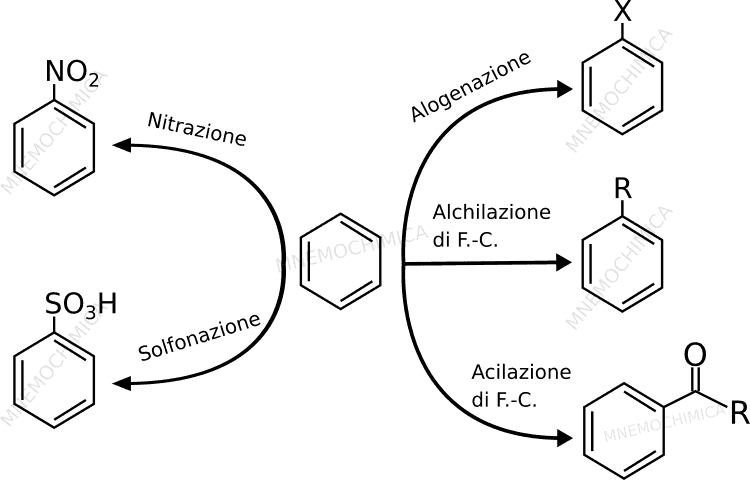
Ovviamente nell’alogenazione, ottieni un prodotto diverso a seconda dell’alogeno che utilizzi. Se parti dal benzene e fai la clorurazione, ottieni un clorobenzene. Viene da se che se utilizzi il bromo (bromurazione) otterrai un bromobenzene. Mentre nell’alchilazione di Friedel-Craft, R è sinonimo di un gruppo alchilico (da qui il nome), come ad esempio il metilico (-CH3), etilico (-CH2CH3) e così via. Mentre nell’acilazione di Friedel-Craft posso ottenere o un aldeide (benzaldeide) oppure un chetone (il più semplice è l’acetofenone).
Ah, devo dirti una cosa importante. Il prodotto (che vedi nello schema sopra) della solfonazione del benezene, si chiama acido benzensolfonico. Te lo dico perché molti si confondono.
Meccanismo di Reazione della Sostituzione Elettrofila Aromatica
Il meccanismo di reazione della SEA è molto semplice, in poche parole l’effetto finale è quello di sostituire un idrogeno (legato al composto aromatico) con un elettrofilo.
La differenza tra le varie reazioni, sta nell’elettrofilo (e ovviamente nei composti che utilizzo per prepararlo), poi per il resto la reazione è sempre più o meno la stessa.
Nel dettaglio, ti spiego sotto i 3 punti chiave.
#1 Addizione dell’elettrofilo
Ti ho scritto il benzene riportando anche gli idrogeni che in genere invece si omettono (li scrivo in leggera trasparenza). Il benzene utilizza 2 elettroni del sistema aromatico per legare l’elettrofilo. Così facendo però “distrugge” l’aromaticità, che come non finirò mai di dire, conferisce stabilità alla molecola (il termine “distrugge” ovviamente è inter nos, non dire al prof una cosa del genere).
Ricorda che un composto per essere aromatico deve rispettare determinate regole.

#2 Intermedio di Wheland
Come conseguenza dell’addizione, si forma il carbocatione (chiamato intermedio di Wheland), dove la carica positiva risuona nelle posizioni orto, para e di nuovo orto rispetto all’elettrofilo che hai appena aggiunto, come vedi in figura.
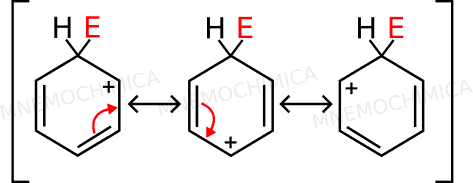
#3 Ripristino dell’aromaticità
Nell’ultimo passaggio, si ripristina l’aromaticità che – come ti ripeterò 1 miliardo di volte – è un processo molto favorito (perché l’aromaticità conferisce una forte stabilità alla molecola e nella chimica si va sempre verso la maggiore stabilità).
Come torna ad essere aromatico il composto nella SEA? Grazie ad una base che va a deprotonare (“togliere” un idrogeno) al benzene. Gli elettroni di legame tra il benzene e l’idrogeno, li prende il benzene e li usa per l’appunto per ripristinare il sistema Aromatico.

Questa era una semplice spiegazione su cos’è la sostituzione elettrofila aromatica. Come vedi, non c’è assolutamente nulla di difficile da ricordare.
Se il benzene ha già un sostituente?
Devi sapere quando il benzene è già sostituito (es: clorobenzene) e lo faccio reagire per SEA, il nuovo gruppo si legherà in punti precisi (e non a caso), quindi fai molta attenzione quando devi sintetizzare un benzene polisostituito.
Per approfondire puoi vedere l’articolo sulle posizioni orto, meta e para. Ma ti faccio un riassunto qui.
Ci sono due possibilità:
- gruppi che orientano in orto e in para (es: alogeni);
- gruppi che orientano in meta (es: nitro, carbossilico, ecc);
Che significa? Se ad esempio faccio una qualsiasi reazione di sostituzione elettrofila aromatica su un clorobenzene, ottengo 2 prodotti. Il “nuovo” elettrofilo si legherà sia in posizione orto che in posizione para rispetto al cloro…